近日,中科院合肥研究院健康所(中国科学院合肥肿瘤医院医研融合一体化发展单位)刘青松药学团队与美国哈佛大学医学院Dana-Farber癌症研究所James Griffin教授团队合作,发现了针对EZH2突变阳性恶性血液肿瘤的治疗新靶点USP47。该研究成果在线发表于国际医学著名期刊Leukemia。
在恶性血液肿瘤如生发中心弥漫大B淋巴瘤(GCB- DLBCL),滤泡性B细胞淋巴瘤(FL)及急性髓系白血病(AML)中,分别大约有22%-24%,10%和1%的患者携带EZH2-Y641位点的突变。该突变一方面可导致组蛋白甲基转移酶EZH2高度活化,催化组蛋白H3在赖氨酸27位的三甲基化修饰(H3K27me3)来介导基因沉默;另一方面通过影响EZH2的转录因子活性来调节下游信号通路,最终导致恶性血液肿瘤的异常增殖和进展。因而单纯使用EZH2甲基转移酶活性抑制剂不能起到较好的抑制肿瘤生长的疗效,且因长期用药易导致二次突变引起耐药,增加不良预后,这也是弥漫大B淋巴瘤等对近期获批或者在临床试验中的EZH2抑制剂响应率低或者耐药的主要原因。因此,针对EZH2突变型的恶性血液肿瘤开发新型治疗策略具有重要的临床意义。
在本研究工作中,科研人员通过高通量筛选发现结构相近的两个化合物P22077和1247825-37-1可以选择性抑制EZH2-Y641C突变的AML细胞系的增殖,并且能够选择性降解EZH2-Y641C蛋白而对野生型没有作用,这种选择性抑制和降解作用在更具有临床治疗意义的突变型DLBCL细胞中也得到了验证。通过多组学分析研究发现,这两个化合物抑制了去泛素化酶USP47的酶活,影响了突变EZH2蛋白的泛素化水平,进而导致突变型EZH2的降解,破坏EZH2相关信号通路的活化。此外,通过基因编辑等分子生物学技术研究发现,USP47在EZH2突变型DLBCL中高表达,更倾向于和突变型EZH2结合,从而增加其蛋白稳定性。酶活抑制和基因沉默USP47均能够有效抑制DLBCL细胞系的增殖,而对正常人外周血细胞(PBMC)没有明显作用。在原代病人细胞以及动物肿瘤模型上的药效评价结果显示,USP47抑制剂能够有效诱导原代病人细胞内突变型EZH2蛋白的降解以及细胞的死亡,从而抑制肿瘤的生长。以上研究结果表明,靶向USP47是针对EZH2突变的恶性血液肿瘤的潜在的治疗手段。
该研究获得了国家自然科学基金、安徽省自然科学基金等项目的支持。
文章链接:https://www.nature.com/articles/s41375-021-01494-w
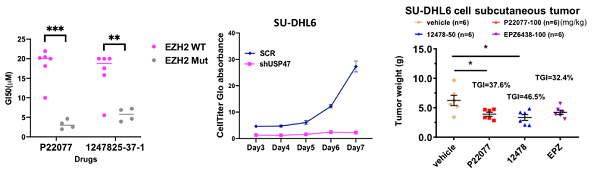
体内体外酶活和基因水平上抑制USP47均可显著抑制EZH2突变型细胞增殖






