近日,中科院合肥研究院健康所(中国科学院合肥肿瘤医院一体化发展单位)刘青松药学团队基于药物重定位策略,通过高通量药物筛选方法,发现临床II期FGFR抑制剂AZD4547通过选择性抑制RIPK1发挥强效抗坏死作用。该研究成果在线发表于药学期刊Acta Pharmacologica Sinica。
细胞坏死(Necroptosis)是一种程序性的细胞死亡过程,主要表现为细胞肿胀和细胞膜破裂。伴随着细胞坏死的发生,胞内大量内容物快速释放,造成机体产生强烈的炎症应答。越来越多的研究表明,细胞坏死参与了多种病理过程,包括炎症、感染和神经退行性疾病等,因此抗坏死抑制剂的开发近年来成为研究热点。受体相互作用激酶1(RIPK1),受体相互作用激酶3(RIPK3)和混合系激酶区域样蛋白(MLKL)在细胞程序性坏死的过程中发挥重要作用,因此这三个靶点成为抗坏死抑制剂开发的主要方向。目前,基于后两者进行的小分子药物开发由于潜在的靶点毒性和不佳的药代性质,尚无药物进入临床研究,而以RIPK1为靶点发展的小分子抑制剂在多种动物模型上展现出良好的作用效果和安全窗口,已有药物进入临床试验阶段。
在本研究中,科研团队采用“老药新用”的药物研发策略,通过对目前已上市和处于临床试验中的药物进行基于表型的高通量筛选,发现了一种选择性FGFR抑制剂AZD4547具有强烈的抗坏死活性。在细胞坏死模型中,该化合物能够剂量依赖性地抑制细胞坏死的发生。进一步的机制研究发现,AZD4547通过选择性地抑制RIPK1,进而抑制坏死相关信号通路的活化来发挥抗坏死功能。体外酶动力学实验和分子对接结果表明,AZD4547作为非经典的II型ATP竞争性抑制剂与RIPK1结合。此外,在肿瘤坏死因子-α(TNFα)诱导的全身性炎症反应模型(SIRS)中,AZD4547在较低剂量下能够在保护小鼠体温、提升小鼠存活率以及抑制小鼠体内细胞因子风暴等方面显示出良好的作用效果。这些研究结果表明,AZD4547有望在坏死相关炎症疾病的治疗中发挥作用。
该研究工作获得了国家自然科学基金、中科院前沿科学重点研究计划和中科院青促会等项目的支持。
文章链接:https://www.nature.com/articles/s41401-022-00993-5
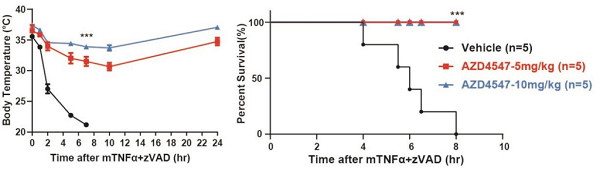
AZD4547在TNFα诱导的SIRS小鼠模型中发挥保护作用






